Ⅰ. 서론1)
혁신적 개발재원(Innovative development financing, IDF)에 대한 논의는 2002년 몬테레이에서 개최된 1차 개발재원회의를 시작으로 구체화 되어왔다. 2004년 9월 ‘혁신적 개발재원 조달 매커니즘에 관한 전문가 그룹 보고서’는 금융거래세, 무기거래세, 국제금융기금(International Financial Facility), 개발재원 특별 인출권 등의 다양한 재원 마련 방식을 제시하였으며, 2005년 9월 유엔 특별 정상회의에서 채택한 '개발을 위한 혁신적 재원 조달에 관한 선언’은 ODA의 보완재로서 혁신적 개발 재원의 역할을 강조하고 국제 조세의 신설, 구체적으로는 항공권 연대 기여금 프로젝트에 대한 지원을 발표하였다(오수현, 2016: 32-36).
이후 2006년 ‘혁신적 개발재원 파리 각료급 회의’에서는 항공권 연대 기여금의 강화와 이 기여금을 감염병 퇴치를 위해 사용하는데 합의했고, 이를 계기로 ‘개발을 위한 혁신적 개발재원 조달 리딩 그룹’이 창설되었다. 보건 개발 분야에 기여금을 활용하는 것을 목표로 2006년 국제금융면역백신기구(International Finance Facility for Immunization, IFFIm), 국제의약품구매기구(UNITAID)를 설립, 항공권 연대기금을 포함 선시장약정(Advance Market Commitment, AMC), debt2health 등의 재원 조달 방식이 실행되었다(김태균, 2012: 89-91).
2007년 제3대 혁신적 개발재원 조달 리딩 그룹의 의장국이었던 한국은 프랑스와 더불어 항공권연대기여금을 도입, 국제빈곤퇴치기여금(이하 기여금) 운영을 시작하였다. 이 기여금은 2017년 국제질병퇴치기금(이하 기금)으로 전환되어 개발도상국의 감염병 예방과 퇴치를 중점 지원해오고 있다. 「감염병의예방및관리에관한법률」에 명시된 1~4급 법정 감염병 중 개발도상국의 질병 부담이 높은 감염병(호흡기 질환, 수인성 질환, 말라리아 등)에 대한 예방과 퇴치를 목적으로 한다. 기금은 초기 모자보건 위주의 사업에서 감염병 예방 및 대응 분야로 사업을 확장하여 왔다.
국제사회는 그간 HIV/AIDS·결핵·말라리아를 포함, 빈곤연계질병(poverty-related disease)의 퇴치를 위해 노력해왔다. 그 결과, HIV/AIDS로 인한 사망자 수는 2006년 1.95백만 명 대비 2017년 0.95백만 명으로 51% 감소했고(GDB 2017 HIV Collaborators, 2019: 16), 결핵 유병률은 연평균(2000~2018) 1.6% 감소, 사망자 수 또한 11% 감소 추세를 보였다(WHO, 2018: 3). 소아마비(Polio) 및 소외열대질환인 기니아충증은 퇴치(eradication) 단계에 가까워지고 있다.
이러한 성취에도 불구하고, 에볼라·라싸열 등 신종 감염병의 출현, 약제내성균의 확산, 감염병 동시감염, 소외열대질환에 대한 백신 및 치료제의 부재 문제는 개발도상국의 취약한 보건시스템과 결부되어 국제사회의 공조 없이는 해결하기 어려운 복잡성을 띄게 되었다. 이에 국제사회는 특정 질병 중심의 수직적 접근 혹은 보건 시스템 강화에 중점을 둔 수평적 접근의 양자택일 방식을 넘어 보다 통합적(diagonal)인 접근 방식을 강조하고 있다(Kim et al., 2013: 2).
빈곤 등 사회경제적 결정 요인에서 비롯한 낮은 의료서비스 구매력 역시 의료 접근성을 약화시키고, 의료 불평등의 문제를 낳는다. 특히 개발도상국에 만연한 소외 질환에 대한 의약품 개발은 10년 이상의 시간과 비용(백신 1개당 US$ 1~1.5 billion 이상)이 소요된다. 시장성 부족, 의약품 개발 자체의 위험도도 높기 때문에 제약회사 등 민간의 자발적 공급을 기대하기 어려운 실정이다.
이러한 감염병 예방과 퇴치의 장애 요소를 극복하기 위해 한국은 기금을 활용하여 국제사회와 공조하고 있다. 그러나 3년 단위의 짧은 사업 기간과 약 850억 원(국회 예산정책처, 2019: 5) 규모의 연간 자금으로 감염병 퇴치의 가시적 성과를 내기란 어려운 일일 것이다. 사업 방식에 있어서도 한국이 독자적(stand-alone)인 사업을 추진하는 것은 질병 감소라는 장기적 과제를 해결하기에 비효율적이다. 따라서 한정된 재원을 어떤 질병에, 어떤 사업 방식으로, 어떤 수행자를 통해 배분하고 사업 효과성을 높일 것인가에 대한 심도 있는 고민이 필요한 시점이다.
혁신적 개발재원에 대한 기존 선행 연구는 국제 개발 금융의 큰 흐름에서 개발 재원의 의제설정, 동원 및 수단과 연계된 연구에 집중되었다(김태균·이승철·최나은, 2015; 박수영·오수현, 2015; 정지원·정지선, 2011; 현민, 2017). 개발재원 마련의 이행 수단으로서 항공권연대기금에 대한 구체적 연구는 기여금 도입 단계에서 그쳤던 것으로 보인다(윤나미, 2007).
본고에서는 그간의 기여금 및 기금 사업의 진행 상황을 살펴보고, 개발도상국 주민의 건강한 삶에 효과적으로 기여할 수 있는 사업 수행 방식에 대해 검토하고자 한다. 기존 보건 사업과 차별화되면서도 같은 지원 금액으로 더 많은 수혜자에게 혜택을 줄 수 있는 두 가지 대안으로서 국제보건이니셔티브에 대한 비지정 기여 지속 확대와 국제의약품개발파트너십(Product Development Partnership, 이하 PDPs)과의 협력을 제안한다. 이후 영국국제개발부(DFID)의 사례를 살펴보고, 향후 기금 사업에 적용 가능한 시사점을 도출하고자 한다.
Ⅱ. 국제질병퇴치기금의 지난 10년
2004년 이후 국제사회는 MDGs 달성을 위해 개발재원 확보를 위한 노력을 본격화하였다. 이 흐름 속에서 2005년 유엔 특별정상회의 시 한국은 빈곤과 기아문제 해결을 위한 지원을 약속했고, 2006년 초부터 관계부처 간 협의를 통해 항공권 연대기금 도입 방안을 논의하였다(박강호, 2006: 7). 같은 해 정부는 ‘아프리카 개발을 위한 한국 이니셔티브’ 공약을 이행하기 위한 수단으로서 항공권 연대기금 활용을 검토하였으며, 타 공여국 대비 미흡한 ODA 규모(2005년 GNI의 0.09%) 보완, 아프리카 등 최빈개도국의 빈곤 및 질병 퇴치에 공조해야 한다는 필요성 하에 기여금을 도입하였다(박강호, 2006: 9-10).
국제빈곤퇴치기여금은 2007년부터 2016년까지 10년간 약 1,400억 원 규모로 사업을 추진하였다. 국별 협력사업, NGO 협력사업, 국제기구 협력사업 등 다양한 형태의 방식으로 사업이 추진되었다. UNITAID, GAVI에의 비지정 기여를 제외하고 총 32건의 사업 중 모자보건 분야 16건(50%), HIV/AIDS 4건(12.5%), NTD 4건(12.5%), 말라리아 2건(6.2%)의 사업이 진행되었다. 사업 수행자는 NGO(20건/62.5%) 및 국제기구(6건/18.75%)가 대부분을 차지하였다(<표 1> 참조).
MDG 목표 중 가장 달성이 미진했던 유아사망률 감소(MDG4)와 임산부 건강 개선(MDG5)을 위해 탄자니아, 우간다, 모잠비크 등을 중심으로 모자보건 사업을 추진하였다. 구체적 사업 내용으로는 보건 인식 개선을 위한 대중매체 활용 캠페인 및 워크숍 개최, 보건소 신축, 보건지소 증설 등 의료시설 및 의료 서비스의 개선 등이었으며, 지역사회 모자보건서비스에 대한 질적 제고와 접근성 향상을 주요 목표로 하였다.
비지정 기여의 형태로는 UNITAID 집행이사국 활동, 세계백신면역연합(GAVI) 이사회 참여 등 보건 분야의 전문성을 가진 국제기구와의 파트너십을 신규로 구축하였다(국제개발협력위원회, 2017: 139). 국제기구를 통해 백신 및 치료제 개발과 같은 혁신적 사업을 지원해온 결과 6,200만 명의 아동을 대상으로 예방접종을 실시하였고(GAVI, 2017), HIV/AIDS 자가진단비용 96% 인하, 145개국을 대상으로 결핵 진단 비용을 40% 인하(US$17→$9.98)하는 등의 성과를 거두었다.
기존의 기여금은 KOICA의 보건 ODA 사업 형태와 유사한 사업을 추진하면서 ODA를 보완하는 역할에 집중하였다고 볼 수 있다. 국별 사업 및 NGO 사업은 사하라이남 아프리카 국가를 대상으로 보건 시설, 물자 및 인력 지원을 통해 지역사회의 아동 및 모자보건 서비스 접근성 향상을 중점 지원하였다. 특히 규모가 크고 장기적인 사업을 통해 지역사회의 수요에 맞는 분야를 발굴하고, 질병의 예방에 대한 교육과 인식개선의 효과를 가져왔다(한국국제협력단, 2011). 글로벌 보건기구에의 지원 역시 소규모 지원으로도 의약품 개발과 보급에 대한 국제적 성과를 공동으로 가져갈 수 있었다는 점에서 긍정적인 평가를 받았다(한국국제협력단, 2011).
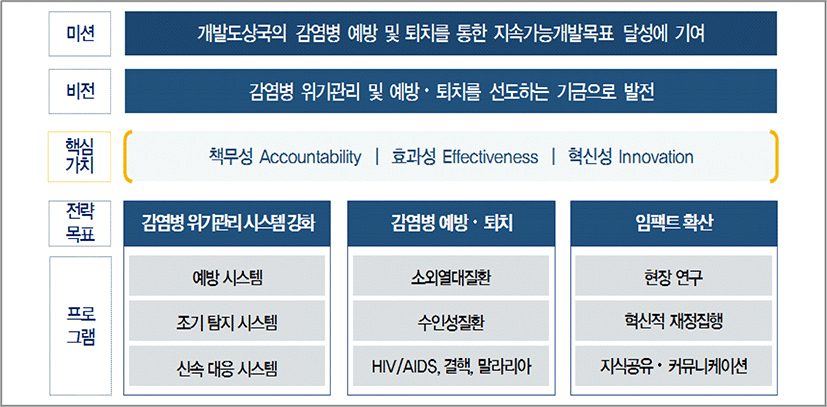
2017년 기금화 이후 전략 방향은 ① 감염병 위기관리 시스템 강화, ② 수인성 질환, 소외열대질환 등 감염병 예방 및 퇴치, ③ 감염병 연구 및 지식 확산의 세 축으로 구성되었다(<그림 1> 참조).2) 사업 주체는 NGO 및 국제기구이며, 국제기구와의 협력 사업 비중이 기여금 대비 증가하였다(<표 2> 참조). 2019년 총 사업비 395억 중 민관협력사업 53억 원(13.4%), 국제기구협력사업 154억 원(39%), 글로벌협력사업 159억 원(40%)에 배분되었다. 주요 분야로 글로벌 보건안보 강화(감염병 위기대응체제 강화, 항생제 내성 대응 등), 수인성 질환 및 소외열대질환 예방 및 퇴치 사업을 추진하고 있다.
즉, 기금의 설립 목적에 부합하는 감염병 사업을 중심으로 개발도상국의 보건 시스템 강화(수평적 접근)와 더불어 감염병의 예방 및 치료 등의 분야(수직적 접근)를 모두 포함하는 통합적 방식으로 방향성이 전환되었다. 사업 수행자 측면에서도 국제기구와는 정책 수립 및 가이드라인 마련 등 국가 단위 혹은 글로벌 차원의 접근이 필요한 사업을 추진하고, 주민 행동변화 유도와 같은 커뮤니티 기반 접근이 필요한 사업은 NGO와 협력하고 있다. 또한, 기금은 예산의 절대적 규모를 고려, 증거 기반의 사업의 구성을 통해 적은 재원으로 효과가 높은 사업 수행 방식이 필요함을 강조하였다(한국국제협력단, 미간행, 2017: 9).
한편, 감염병 분야의 사업 효과성을 제고하기 위해서는 환경 개선, 보건시스템 강화를 포함한 예방-진단-치료의 통합적 접근이 필요하다. 특히 백신, 진단, 치료제에 대한 기술 개발이 지속되어야 사업의 비용대비 효과성을 높일 수 있다. 지난 25년간 빈곤연계질병에 대한 의료 기술 개발은 전체 혁신 기술 개발의 1%만을 차지하였으며, 이로 인해 개발도상국의 의료 접근성 약화 및 관리 비용 증가, 비효율성 문제를 가중시켰다(Howitt, 2012: 508).
예를 들면 효과적 말라리아 퇴치를 위해서는 예방의 관점에서 화학요법(살충제)을 통한 모기 매개체 관리나 약품 처리된 모기장을 지원하고, 정확하고 신속한 말라리아 진단 및 치료도 병행해야 한다. 그러나 기존의 예방법들이 완벽하지 않고, 상황에 따라 제한적으로 사용되며, 재감염을 억제할 수 없기에 새로운 기술의 개발이 필요한 것이다(Bulc & Rohit, 2017; Shiff, 2002: 278-293).
1996년 국제 에이즈 백신 이니셔티브(International AIDS Vaccine Initiative)를 시작으로 국제사회는 감염병 예방과 대응을 위한 효과적 기술 개발과 연구를 지속하였다(Jamison et al., 2013). 일례로 열대열 말라리아(uncomplicated P falciparum) 대응을 위한 아르테미니신 병용 요법(Arteminisin-based combination) 개발은 90%의 치료 효과를 갖는 치료법 접근을 가능케 했다(Howitt et al., 2012: 514). HIV/AIDS 복합제 신약(fixed-dose combination) 개발은 1인당 치료비를 절감하고, 커버리지 역시 확대하였다. 신속 내성결핵 진단 요법의 발전 역시 결핵 유병율 및 사망률을 낮췄다(Howitt et al., 2012: 515).
우리 정부의 유일한 감염병 전문 기금3)으로서 국제질병퇴치기금은 사업의 효과성을 높일 수 있는 사업 방식을 고려할 필요가 있다. 또한, 기존의 KOICA의 보건 ODA 사업과 차별성을 갖기 위해서는 모자보건, 보건위생교육 지원 외에 진단 및 치료제 분야로의 사업 다각화가 필요하다. 그러나 법률상 기금의 주요 역할이 신약 개발이나 진단기기 개발에 있지 않은 점, 부족한 재원 규모, 감염병 분야의 전문성 부족으로 기술 개발을 위한 비용 부담과 위험을 기금이 독자적으로 감수하기란 어려운 일이다. 아울러 국회 및 예산당국, 기금 납부자인 일반 국민을 설득하기도 쉽지 않다.
따라서 이를 극복하기 위해 파트너십을 활용한 사업 방식을 생각해볼 수 있다. 첫째, 감염병 대응을 위해 마련된 국제보건이니셔티브에 참여하거나, 둘째, 대학·산업계·연구계·국제기구 등과의 파트너십을 기반으로 한 플랫폼 형태의 사업을 수행하는 것이다. 기여금 때부터 지원해온 UNITAID, GAVI 등 보건 전문기구들과의 협력을 확대하고, 이미 구축된 감염병 분야의 네트워크를 추가로 활용한다면 감염병에 대한 기술개발 지원도 불가능한 것이 아니다. 제한적인 재원으로도 파급 효과를 높이고, 효율적으로 사업을 수행할 수 있는 대안이 될 수 있다. 파트너십은 부족한 추가적인 재원의 확보, R&D 분야 정보 공유, 기술개발에의 리스크 공유, 수요 기반의 기술 개발을 가능하게 한다(Yamey, 2018: 1-2).
Ⅲ. 국제보건이니셔티브 참여 및 Product Development Partnerships 지원
2000년 전후 발족된 국제보건이니셔티브(Global Health Initiatives, 이하 이니셔티브)는 특정 질병 또는 선택적 개입(selected intervention)을 중심으로 개발도상국의 감염병(HIV/AIDS, 결핵, 말라리아, 백신으로 예방 가능한 질환 등)을 지원하는 파트너십이다(WHO, 2009: 2140-2141). 대표적으로는 글로벌펀드, GAVI, AIDS 구제를 위한 대통령 긴급 계획(PEPFAR), 세계은행 다분야 AIDS 프로그램(World Bank Multi-Country AIDS Program, MAP)을 들 수 있다. 대규모 재원 조달, 성과 기반의 투입, 개발도상국 정부 직접(예산) 지원, 시민사회의 참여 등을 주요 특징으로 한다(WHO, 2009: 2141). 기금 역시 2007년부터 GAVI와 UNITAID, 2013년부터 글로벌펀드를 추가 지원하며 이니셔티브에 참여하고 있다.
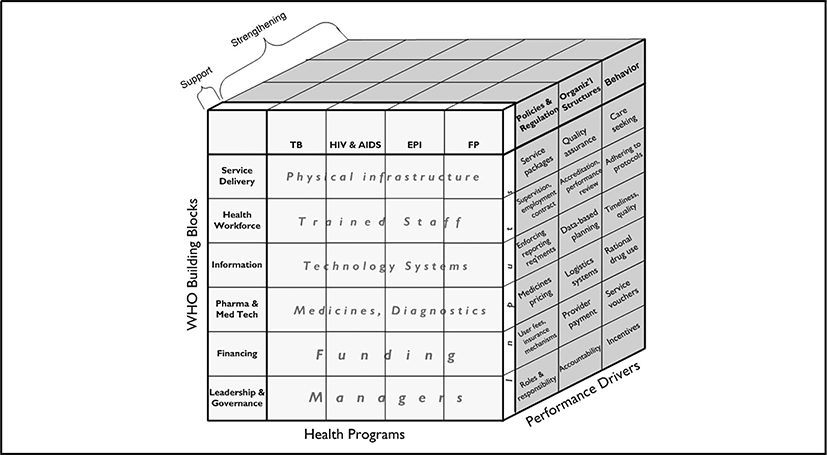
이니셔티브는 개발도상국의 전반적인 보건 시스템 강화와 함께 특정 질병의 퇴치를 목적으로 한 활동을 통합 지원한다. WHO(2009: 2142-2143)는 이니셔티브의 지원이 보건 시스템을 구성하는 6대 요소(보건 서비스 전달, 보건 재정, 거버넌스, 보건 인력, 보건 정보 시스템, 의료 공급망)와 연계하여 각기 다른 부분에서 효과를 가져왔음을 밝힌 바 있다. 또한 Warren et al.(2013: 5)의 글로벌 펀드 지원 분석 결과는 3대 질병 퇴치를 중심으로 한 보건시스템 강화에 37%의 재원이 쓰였고, 특히 보건서비스 커버리지 확대, 보건 인력 강화, 의약품 및 혁신기술 확산에 집중 기여하였음을 보여주었다. 다시 말해 이니셔티브가 타겟 질병에 관한 의료 서비스의 접근성 및 질적 향상, 혁신 기술 도입에 긍정적인 영향을 가져온 반면, 타겟이 아닌 질병과 연계된 요소에 대해서는 다소 제한적인 결과를 가져왔음을 알 수 있다(WHO, 2009; Biesma et al., 2009; <표 3> 참조).
출처: WHO. (2009).
KOICA가 수행해온 프로젝트형 사업은 특정 지역에의 투입(병원 건립, 보건인력 교육, 의료물품 배포 등)을 통해 보건시스템을 지원하는 경우가 많다. 그러나 이니셔티브를 통해 보건 시스템 ‘강화(strengthening)’를 체계적으로 지원하는 것은 보다 포괄적인 수준에서 개발도상국의 보건 정책과 규정, 조직 구조, 효율적인 자원 배분에의 변화를 이끌 수 있다. 즉, 시스템 차원의 개선은 보다 장기적 관점에서 보건 문제에 대한 유연한 대응을 가능하게 한다(Chee, 2012; <그림 2> 참조). 물론 수원국의 주인의식과 원조 조화 등의 측면에서는 3대 감염병을 중심으로 한 이니셔티브 지원의 한계점이 노출될 수 있다. 실제로 더 높은 질병 부담을 지닌 질병보다 이니셔티브의 지원 방향에 맞는 질병만 우선시 되거나, 유사 목적을 가진 재원들의 중복 지원으로 개발도상국 정부의 계획 수립 및 재원 조정 기능이 복잡해지는 경우도 배제하기 어렵다(Biesma et al., 2009; Schwank, 2012).
그러나 보건 시스템의 강화가 뒷받침되지 않고서는 특정 지역에 한정된 사업 효과와 지속성을 보장하기 어렵다. 일부분이지만 3대 질병을 중심으로 한 보건시스템 강화 사업들은 르완다, 아이티 등 많은 국가에서 긍정적인 누출 효과를 가져왔다. HIV/AIDS 퇴치 중심의 보건 서비스 전면 확대, 인프라 구축이 커뮤니티의 산전후 서비스 이용 증가와 같은 다른 보건 서비스 제공도 확대하는 효과를 낳았다(WHO, 2009). 또한, 공여국의 보건 재정 원조가 유동적인 점, 공여국 간 조정 절차가 높은 거래비용을 수반하는 점(Manning, 2008)을 고려할 때, 이니셔티브를 통한 지원은 개발도상국 보건의료 재정의 예측성과 지속가능성을 높이고, 전반적 보건 시스템 강화에 기여하는 등 지원 대비 효과성을 높일 수 있다.
기금의 주요 전략 목표인 감염병의 예방과 퇴치, 위기대응 시스템 강화를 달성하기 위해서는 시스템 차원의 지원이 뒷받침되어야 한다. 이는 한 공여국의 지원을 통해 개선하기 어려운 문제이며, 80개가 넘는 이니셔티브가 상호 공조를 통해 지원해왔다(WHO, 2009). 따라서 기금이 지원해온 이니셔티브에의 참여를 유지하고, 새로운 이니셔티브 참여를 확대해 나갈 필요가 있다. 특히 기금은 의제 설정 등 정책 결정 과정에 적극 참여해야 한다. 풀펀딩을 통한 이니셔티브 참여는 사업 운영 측면에서 감염병 분야 전문 인력과 재원에 대한 규모의 경제를 실현할 수 있다.
또한, 조달 등 개별 프로젝트 관리 및 성과 도출에 따른 거래비용 완화만이 아니라, 개발도상국 보건 시스템 전반에 대한 개선의 효과를 가져올 수 있다. 개별 프로젝트에 대한 공여 기관별 고유의 성과를 평가하기에는 한계가 있으나, 개발도상국의 감염병 예방과 대응은 한 공여 주체가 아닌 국제사회의 공조에 기반을 두므로 성과 역시 공동의 것이 될 수밖에 없음을 감안할 필요가 있다.
PDPs는 소외질병 또는 빈곤연계질병에 필요한 의약품에 대한 진단, 생산, 공급을 목적으로 하는 민관협력의 한 형태이다. 즉, 공공, 비영리단체, 민간산업 및 학계 간 플랫폼으로 정의할 수 있다(이정협 외, 2012). PDPs 내 기관들은 소외열대질환처럼 투자 요인이 낮은 감염병 관리에 필요한 기술 개발을 위해 산·학·국제기구 등과 장기적 파트너십을 구축한다. 제약회사와 같은 공급자에는 개발비용 보조, 개발된 의약품에 대한 권리 부여, 일정 규모의 구매 보장 등을 통해 시장 인센티브를 부여하되 낮은 가격으로 의약품을 공급할 수 있도록 한다(Grace, 2010).
주요 PDPs로는 Aeras Global TB Vaccine Foundation (Aeras), Drugs for Neglected Diseases initiative (DNDi), Medicines for Malaria Venture (MMV), European Vaccine Initiative (EVI), Global Alliance for TB Drug Development (TB Alliance) 등이 있다(<표 4> 참조).5) PDPs는 ① 기초 탐색 및 원천 기술 연구, ② 전임상 시험, ③ 임상 1, 2, 3상, ④ WHO·EMA 등의 허가·승인 절차를 지원하고, ⑤ 개발된 백신과 치료제 등이 개발도상국에 도입될 수 있도록 한다(<표 5> 참조).
DNDi, Drugs for Neglected Diseases initiative; FIND, Foundation for Innovative New Diagnostics; MMV, medicines for malaria venture.
출처: ‘Aerts et al., 2017’ 및 ‘FIND, TB Alliance, MMV, DNDi 홈페이지’.
PDPs의 대표적 성과로는 MMV-노바티스사 파트너십을 통해 개발한 어린이용 항말라리아제, PATH의 A형 뇌척수막염균 백신(MenAfriVac) 개발 및 백신가격 인하(0.5달러 수준), DNDi의 소외열대질환(아프리카 수면병, 리슈마니아증) 치료제 개발, MMV-DNDi가 협력한 항말리리아 복합제 개발, Malaria Vaccine Initiative와 GSK의 협력을 통한 말라리아 백신(RTS, S) 개발 등이 있다6).
이 혁신 기술들은 개발도상국에서 소외 질환으로 사망하는 인구(특히 5세 미만 아동)를 줄이는데 결정적으로 기여하였으며, 약품 가격을 낮춤으로써 구매력이 낮은 개발도상국 주민의 의약품 접근성을 향상시켰다. 예를 들어 치사율이 100%인 아프리카 수면병의 경우, DNDi가 개발한 치료제(NECT)로 99% 이상이 치료될 수 있는 것이다(Boulton et al., 2015: 15). 비록 데이터가 부족하기 때문에 정확한 장애보정생존연수(Disability-Adjusted Life Year) 등을 기준으로 한 건강 증진 성과를 측정하기는 까다로우나, 개발도상국 주민이 건강한 삶을 얻게 됨으로써 얻을 수 있는 사회경제적 효과는 막대하다.
아울러 PDPs는 하나의 제도로서 기능하면서 공공보건 분야의 혁신과 의료 접근성 확대를 이끌어내는 역할을 맡고 있다(Boulton et al., 2015: 1-3). 협력 인센티브가 없었던 파트너 간 협력을 촉진하여 백신 및 진단기기 등을 연구·개발하고, 공공조달을 활용하여 기술 확산을 이끈다. 개발도상국 내에서의 기술 도입 지원, 의약품 규제 강화, 국제적 수준에 맞는 의약품 생산 지원, 의약품 및 진단기기 가격 인하 및 라이센싱 확보를 직·간접적으로 돕는데 그 혁신성을 지니고 있다(Boulton et al., 2015: 4; Mahoney, 2011).
PDPs 기관의 설립 목적 및 공여 주체가 공공성을 띄기에(자선 재단, 공여국 중심) 취약 계층에 대한 의료 서비스의 공공성 확보를 우선순위화 할 수 있는 근거를 마련한다. 더 나아가 지속가능개발목표(Sustainable Development Goals) 3(건강한 삶) 중 3.3(3대질환 및 소외열대질환 등 퇴치), 3.8(보편적 의료보장), 3.b(백신 및 의약품에 대한 연구개발 및 의료 접근성 확보)의 지표 달성과 직결된다.
국제질병퇴치기금 역시 혁신 기술의 개발부터 개발도상국 도입 과정의 여러 단계 중 특정 단계에서 선택적으로 PDPs와 협력하여 혁신적 역할을 수행할 수 있다. 예를 들어 PDPs를 통해 개발 및 승인이 완료된 백신 및 치료제를 개발도상국의 의약품 목록에 등록하고, 국가 내 도입을 지원하는 실행단계에서의 기금과의 협력방안을 생각해볼 수 있다.7)
Ⅳ. 영국 국제개발부(DFID)의 PDPs 지원 사례
DFID는 PDPs 펀딩 그룹8)의 일원으로서 빌엔멜린다게이츠 재단(6,400억 원, 16%)과 더불어 PDPs의 주요 도너 역할을 해왔다. 개발도상국에 필요한 R&D분야의 비용과 위험 때문에 민간산업분야가 국제보건 문제에 신속히 대응하지 못하는 점을 고려, 이를 해결하기 위한 수단으로 국제기구 펀딩을 통해 PDP를 지원해온 것이다(이미정 외, 2015: 87). DFID는 2017년 기준, 소외 질환에 대한 전체 3,566백만 달러(약 4조 1천 억 원) 지원액 중 100백만 달러(약 1,160억 원, 2.8%)을 투자하였다(G-FINDER, 2019: 95)9). 특히 2015년에는 1억 유로(1,300억 원)를 투자하여 보건부와 함께 ROSS FUND를 설립하고 항생제내성, 에볼라 등 신종 감염병, 소외열대질환을 중심으로 백신, 진단, 치료제 개발을 지원에 앞장서고 있다(DFID, 2016).
2019년 10월 기준 DFID는 ROSS 펀드를 통해 지속가능성을 확보하고, 비지정기여(non-restricted)의 형태로 Path, 옥스포드 대학, MMV, TB alliance 등 총 9개의 PDPs를 지원하고 있다. 그 규모는 2017~2022년 약 3.3억 파운드(5천 억 원)에 달한다(Ross Fund Portfolio, n.d). PDPs와의 협력 사업을 통해 개발된 소외 질환에 대한 백신, 진단기기, 치료제는 개발도상국 수혜자 규모를 확대하고, 의료 서비스의 질적 제고와 접근성을 강화하였다. 예를 들어 말라리아 환자 중 아동이 사망자의 85%를 차지하는 상황에서 DFID의 지원으로 MMV가 아동용 항말라리아제인 코아템을 개발하여 50개국의 3억 8천만 명을 치료하였다(MMV, n.d.).
DFID는 경제성(비용 절감), 효율성(투입 대비 최대 결과), 효과성(투입 대비 목표 달성) 측면에서 PDPs의 활동을 평가한 바 있다(<표 6> 참조). 각 PDPs들이 가진 네트워크를 활용하여 의약품 연구 및 개발을 위한 전문 인력을 확보하였고, 참여 기관과의 매칭 펀드를 통해 비용 절감의 경제적 효과를 가져왔음을 알 수 있다. 또한, 4~5년의 기간에 다양한 진단기기와 신약 개발에 성공하여 그 효과성을 입증하였다. DFID는 PDPs에 대해 보다 장기적인 재정 지원을 권고하고 있으며, 지원 형태로는 예산 집행의 자율성을 보장할 수 있는 비지정 기여의 확대를 제안하였다(Boulton et al., 2015: 36). DFID의 사업 평가 결과는 호주, 네덜란드의 PDPs 사업 평가와도 유사하다.
출처: Boulton et al., 2015.
Ⅴ. 시사점과 향후 과제
영국의 DFID 사례는 세 가지 시사점을 준다.
첫째, 감염병 분야의 전문성 등 양자기관으로서 가질 수 있는 제약사항들을 국내외(보건부·학계·산업계·국제기구 등) 파트너십을 활용하여 극복해왔다는 점이다. 둘째, 비지정 기여 중심으로 지원한다는 점이다. PDPs가 달성해야 할 전략과 비용 대비 효과적(Value for Money)인 사업을 위해 필요한 예산 편성과 집행의 자율성 및 유연성을 부여하고 있다. 셋째, PDPs에 대한 DFID의 장기적 지원에 주목할 필요가 있다.
이를 바탕으로 기금의 향후 과제 역시 세 가지 측면에서 살펴볼 수 있다. 첫째, 기금의 국내외 파트너십 확대가 요구된다. 감염병 전문 기금으로서 고유 영역을 확보하고, 기술 개발을 지원할 수 있는 사업을 기획하기 위해서 UN 기구를 넘어선 파트너십을 구축해나갈 필요가 있다. 즉, 이니셔티브 내에서 의제 설정을 주도하고, PDPs와의 협력을 확대해야 한다. 또한 질병관리본부, RIGHTS FUND, 범정부 감염병 연구개발 사업단 등 감염병 분야의 국내 이해관계자들과도 선제적인 논의를 추진해나가야 한다. 위탁운영 기관으로서 KOICA는 감염병 분야에 대한 전문인력과 막대한 재원을 단기간에 확보하기 어렵기 때문에 타 공여국의 사례와 같이 다양한 파트너십을 통해 한계를 극복해나가야 하는 것이다.
둘째, 기금의 비지정 기여의 확대 노력이 필요하다. 기금은 이니셔티브 지원 사업을 제외하고는 국제기구 및 NGO에 대한 엄격한 기여 형태로 운영된다. 향후 감염병 대응을 위한 기술개발을 지원하기로 한다면 고비용, 고위험의 특성을 갖는 연구개발사업의 성격을 고려하여 사업수행기관이 보다 자율적으로 예산을 운영할 수 있도록 완화된 기준을 제시할 필요가 있다. 현재의 엄격한 지정기여 형태는 타 공여국과의 통일되고 일관된 가이드를 부여하지 않는 이상 효과적으로 사업을 수행하기 어렵다(Boulton et al., 2015: 6).
또한, 연구개발의 특정 단계를 지원하는 것보다 비지정 기여를 통해 의약품 개발 포트폴리오 자체를 지원하는 것이 오히려 위험을 줄일 수 있다. PDPs는 유연한 예산을 활용해 포트폴리오 중 개발 가능성이 낮은 파이프라인(후보물질)은 빨리 포기하고(make fast go/no-go decisions), 개발 가능성 높은 곳에 비용을 투입할 수 있다. 결과적으로 연구개발 도중 발생할 수 있는 매몰비용을 줄이고, 더 많은 파이프라인을 확보할 수 있다. 예를 들어 HIV 및 결핵에 대한 약제 내성이 증가하는 상황에서 충분한 후보물질을 확보하는 것은 향후 대체 약제를 개발할 때 도움이 된다(Mostert et al., 2014: 28-44).
그러나 기금에서 일정 규모 이상의 비지정 기여 사업을 형성하는 것은 성과관리 및 연도별 예산 확보 차원에서 현실적 제약이 있을 수 있다. 이는 국내적으로 유관 부처와의 예산 협의 절차에서 연도별 성과 측정이 필수적이기 때문이다. 따라서 단기적으로 여러 단계 중 혁신 기술에 대한 글로벌 기관의 승인·허가 절차 지원, 개발도상국 도입 단계를 우선 지원하는 것이 대안이 될 수 있다. 의약품 허가, 규제 가이드라인 마련과 같은 분야에서는 PDPs의 전문성에 더해 한국의 식약처와 같은 유관 기관과의 협력 및 전문 인력을 활용할 수 있는 기회도 마련할 수 있을 것이다.
셋째, 기금의 장기 지원을 적극 고려할 필요가 있다. 항공권 부담금의 형태로 조성되는 기금의 특성상 일반 보건 ODA 예산보다 예산의 지속성을 확보할 수 있다는 장점이 있다. 프랑스가 항공권연대기금의 90% 이상을 UNITAID에 기여하는 것과 같이 기금 역시 글로벌펀드나 UNITAID 같은 이니셔티브에 2007년부터 장기적 지원 중이다. 또한, PDPs의 기술개발을 효과적으로 달성하기 위해 타 공여국의 경우 짧게는 5년, 길게는 7~10년 단위의 사업을 제안하고 있다(Mostert et al., 2014). PDPs 역시 작은 규모라도 공여국의 장기적 지원을 선호한다(Boulton et al., 2015: 35). 현 수준에서는 엄격한 지정 기여를 할 수밖에 없다면 장기적 지원을 통해 타협점을 찾을 수 있다.
비지정 기여를 통해 다양한 이니셔티브와 사업을 구성한다 하더라도 향후 기금은 전략을 기반으로 우선순위 및 사업 방식을 설정해야 한다. 다양한 감염병 중에 어떤 질병을 우선순위로 하여 지원할 것인가, 3대 질환(HIV/AIDS·결핵·말라리아)을 중심으로 할 것인가, 소외열대질환을 중심으로 지원할 것인가, 같은 비용으로 더 많은 수혜자를 치료할 수 있는 감염병에 투자할 것인가, 아니면 수혜자는 적지만 치사율이 높고 치료법이 전무하여 기술 개발의 시급성과 수요가 높은 감염병을 우선 지원할 것인가, 3대 질환 중 질환 간, 단계별 포트폴리오를 어떻게 구성할 것인가 등의 정책 결정은 개발도상국의 감염병 문제 수준을 포함하여 기금의 중장기적 방향성 및 궁극적 가치를 어디에 두느냐에 따라 달라질 것이다.
Ⅵ. 결론
감염병, 특히 빈곤연계질병에 대한 투자는 현재와 미래의 국제보건 분야 전반에 영향을 끼칠 수 있는 문제이기에 더 이상 한 국가만의 문제가 아니다. 한국 정부의 유일한 감염병 전문 기금으로서 글로벌 사회적 가치인 SDGs 3(건강한 삶) 달성에 기여하고, 개발도상국 주민의 건강 증진이라는 실질적 성과를 내기 위해서는 비용 대비 효과적인 사업 형성이 필요하다. 이 과정에서 보건 분야의 혁신적 기술 개발에 대한 지원은 감염병의 예방 및 퇴치 과정에서 보다 근본적 해결방안을 제시해줄 수 있다.
본고에서는 기금의 향후 추진 방향으로 단독 사업이 아닌 파트너십에 기반한 이니셔티브 참여 확대와 기술 개발을 위한 민관협력 플랫폼인 PDPs 활용 방안을 제시하였다. 아울러 주요 공여국 사례로서 DFID의 PDPs 지원성과를 제시하였다. 이니셔티브 및 PDPs에 대한 장기적 지원은 사업의 경제성 및 효율성 측면에서 대안이 될 수 있다. 정부 기금이 갖는 제약을 고려하여 현재의 프로젝트 형태의 사업을 유지하면서 연구개발의 여러 단계 중 개발도상국의 혁신기술 도입 지원을 통해 감염병 예방과 대응에 기여할 수 있다.
또한, 유관 부처, 공공기관, 국회, 연구소, 재단 등 감염병 분야의 국내 기관과 파트너십을 더욱 공고히 하여 기관 간 잠재적 역할 및 지원의 중복성, 비효율성을 극복해 나가야 한다. 마지막으로 중요한 것은 기금의 향후 중장기 전략과 방향성이다. 한정된 재원을 어떤 질병(what)에, 어떤 사업 방식(how)으로, 어떤 수행자(who)를 통해 배분하고, 사업 효과성을 높일 것인가에 대한 고민을 바탕으로 현재의 전략을 평가·모니터링하고, 차기 전략을 고도화 한다면 감염병 전문 기금으로서의 역할을 공고히 할 수 있을 것이다.